

在药械组合产品这一日新月异的领域中,组件供应商之间,以及供应商与制药企业之间的协同增效至关重要。尤其在将预灌封注射器(PFS)集成至自动注射器的开发过程中,协作更是不可或缺。此类合作关系远非简单的交易往来,是真正能够提升产品性能、确保符合监管要求并能前瞻性地预见未来需求的战略伙伴关系。成功的合作最终将打造出以患者为中心的药械组合产品,实现"1+1>2"的卓越成效。
随着新行业指南的出台,例如,美国食品药品监督管理局(FDA)针对递送药物和生物制品的器械所制定的《基本药物递送输出指南》(EDDO),企业间的紧密协作对于药械组合产品的成功开发变得比以往任何时候都更为关键。
鉴于每个组件供应商在构建稳健系统中都承担着关键的作用,那核心问题在于:如何为制药合作伙伴减轻研发负担,降低开发过程中的产品失败风险,并加快产品上市速度?针对这一挑战,Gerresheimer、Aptar Pharma 和 SHL Medical 携手合作,共同采集了自动注射器系统(图 1)的功能与性能数据。该系统基于 SHL Medical 的 Molly® 自动注射器平台,集成了 Gerresheimer 高品质的 Gx® Elite 注射器与 Aptar 的 Premium Coat® 胶塞。此次三方合作充分证明:通过共享专业知识并在开发早期生成数据,能够有效简化开发流程,助力制药企业为其药械组合产品实现最优成果。”

确保自动注射器类药械组合产品的合规性与性能
将预灌封注射器(PFS)集成至自动注射器面临着独特挑战,这对精度、可靠性及各组件间的无缝整合提出了很高要求。注射器针筒、弹性体密封件及自动注射装置等每一部件必须协同运作,以保障最终药械组合产品的整体安全性与有效性。在此过程中,组件供应商发挥着至关重要的作用:他们需要依据国际标准对其产品进行严格的测试与验证。这些标准涵盖新发布的《美国药典》(USP)<382> 与 <1382>、针对预灌封注射器的 ISO 11040-8 章节、针对自动注射器的 ISO 11608-1 与 ISO 11608-5 章节,以及美国 FDA 发布的《基本药物递送输出指南》(EDDO)。
USP <382>
本通用章节规定了注射剂包装/给药系统的适用性功能要求,包括部分或全部由弹性材料制成的主要包装组件。针对预灌封注射器(PFS),USP <382> 的规范范畴具体包括:启动力与滑动力(BLGF)、护帽功能、活塞密封完整性以及完整性测试。
ISO 11040-8
ISO 11040-8 是 ISO 11040系列标准的一部分,主要关注药品包装系统及组件,专门规范用于给药的“成品预灌封注射器”。该标准涵盖了预灌封注射器(PFS)在设计、功能性、安全性及材料方面的具体要求,以确保其在使用过程中的安全有效性,并维持产品的完整性。其规范范围包括:尺寸规格、性能测试,以及对医疗专业人员和最终用户至关重要的可用性特征。
ISO 11608-1 与 ISO 11608-5
ISO 11608 系列标准(尤其是第 1 部分和第 5 部分),规定了含针注射系统中自动化功能的性能要求与测试方法。这些标准明确了评估具有自动功能(如药物输送和针头插入)的装置所应遵循的必要标准。其涵盖的关键要素包括:给药机制、性能测试、安全性、可用性及机械性能要求。该系列标准有助于制造商设计与开发可靠、安全的自我给药装置,从而推动监管审批流程,并提升用户对自动化医疗装置的信任度。
美国食品药品监督管理局(FDA)针对递送药物和生物制品装置所制定的“基本药物递送输出指南”(EDDO)
在开发药物及生物制品给药装置时,充分考量基本药物递送输出(EDDO)对于确保产品的疗效、安全性及法规合规性至关重要。对此,美国食品药品监督管理局(FDA)提供了明确的指导原则。供应商可在药械组合产品开发的早期阶段,针对部分 EDDO 指标开展预测试,以降低后续开发负担。重点评估维度包括:给药剂量的准确度与精密度、给药速率、用户界面与可用性、系统的可靠性与稳健性,以及安全性与风险控制措施。
通过系统整合为药械组合产品的成功开发奠定基础
基于对系统物理性能的了解与经验,组件供应商可针对典型使用场景建立合理假设,进而生成具有价值且独立于特定药物的平台数据。该方法通过实施关键性测试,有效验证自动注射器系统及其组件的性能,涵盖以下核心维度:
– 护帽拔出力(PoF):评估在保持无菌性的前提下护帽移除的便捷性。
– 启动力与滑动力(BLGF):利用模拟液复现注射过程中的受力情况。
– 自动注射器适配性:确保尺寸与功能上的兼容性。
通过提供详尽全面的数据支持,供应商能够帮助制药企业无需从零开始研发,即可选择最优组件方案,从而加速开发进程并降低项目风险。除平台开发外,供应商关联实验室或第三方独立实验室还可开展稳定性研究、临床使用模拟及人因工程(可用性)测试。这种前瞻性的协作模式为药械组合产品的成功开发及监管设计验证奠定了坚实基础。
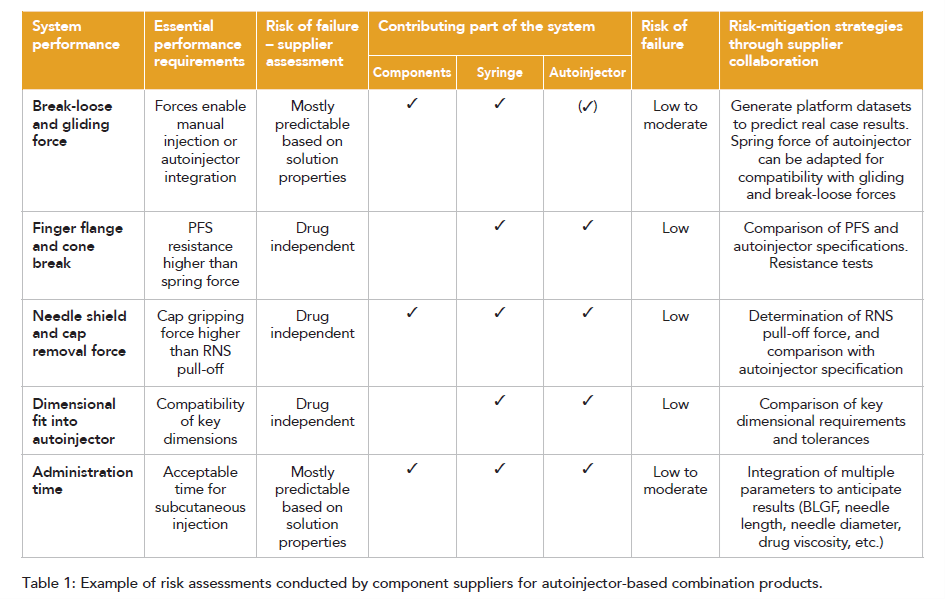
风险评估在系统测试中同样发挥着关键作用。供应商必须评估组件失效的风险,并制定相应的缓解措施。例如,启动力与滑动力(BLGF)通常具有较高的可预测性,自动注射器的弹簧力可根据特定性能要求进行调整(见表1)。
注射器针筒与弹性体组件的接触面
注射器针筒与弹性体组件(包括针头护帽及胶塞)之间的接触面,对器械装置的物理性能至关重要。图1阐述了可能影响该接触面特性的物理因素,这些因素既可能是依赖药物的,也可能是与药物无关的。
USP <382>和USP <1382>章节为这些组件的功能性数据提供了指导。尽管药品上市后的合规终责在于制药企业,但组件供应商仍可先行验证装置中关键且非药物相关的功能。这些测试通常包括使用注射用水或其他模拟液体填充注射器进行范围界定评估,以建立基础性能数据。所谓“范围界定”,即是将性能良好的组合产品作为平台方案推荐给药企,而效果欠佳的组合则不予优先考虑。通过测试和评估不同注射器针筒与弹性体之间的配合度,有助于确定最终将集成至自动注射器中的容器规格。这些平台测试数据对于根据预期用途确定器械装置内的最佳初级包装组合至关重要。例如,来自格雷斯海姆和Aptar Pharma等测试实验室的BLGF曲线,正是助力选择最优组件的关键工具。
注射器特征:非药物相关型与药物依赖型
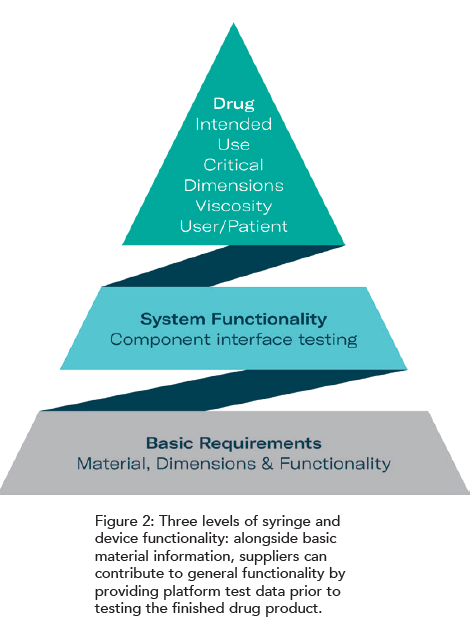
如果组件供应商之间通力协作,各项基本要求的可靠性测试可由组件供应商负责实施。其中,非药物相关测试主要取决于材料属性,完全不受药物特性影响,可由供应商单独执行。系统级要求测试虽受液体理化性质影响,但其本质仍属物理范畴;因此,可采用模拟液进行替代测试,使供应商在接触原料药(API)前即可完成设备系统的适配与优化。此类协作产生的数据,有助于确定最优的注射器系统及自动注射器设计方案。然而,针对预灌封注射器成品或已装配至自动注射器中的注射器,必须开展药物依赖性测试,此类测试仅能在制药企业的实验室内实施(见图2)。
硬质针头护帽(RNS)的拔出力(PoF)本质上与药物无关,取决于以下因素:
– 锥头尺寸
– 针头外径(OD)
– 硬质针头护冒的设计与材料
– 硅化工艺
– 灭菌条件
– 储存时间与条件
作为预灌封注射器的核心参数,启动力和滑动力(BLGF)显著受药液性质影响。具体而言,滑动力的主要影响因素包括:
– 针筒材质
– 针筒长度与内径(ID)
– 针头长度与内径
– 药液黏度
– 弹性体选材与设计
– 硅化工艺及用量
– 加塞方式
– 储存时间与条件
– 测试应用的速度参数
为在缺乏既定药物制剂的情况下评估滑动力,注射器供应商可采用模拟药物特性的模型液来生成导向性数据。
Gerresheimer 与 Aptar Pharma 针对 2.25 mL Gerresheimer Gx® Elite 注射器进行了一系列测试(见图3),以展示该注射器整体的系统性能。自动注射器通常在低温环境下储存,例如在使用前存放于患者的冰箱中。在这种情况下,拔除护帽可能会导致不可接受的高拔出力(PoF)。测试表明,在优化了锥体与弹性体的接触面后,5°C 的储存条件对拔出力没有显著影响。在优化锥头/硬质针头护帽(RNS)接触面后,对硬质针头护帽拔出力(RNS PoF)进行了测试:室温下的平均值为 10.59 N,而在 5°C 冷藏储存条件下的平均值为 12.16 N。这些结果被视为优异,因为目前预灌封注射器(PFS)的标准拔出力值通常在 30 N 或更高。

预灌封注射器与自动注射器的接口
实现预灌封注射器针筒与自动注射器的无缝集成至关重要,这直接决定了最终组合产品的功能性、安全性及可靠性。部分性能参数与药物无关,可在开发早期进行预先评估。此类参数包括:针头护帽拔出力、激活力以及各组件间的整体机械兼容性。相比之下,更多关键的功能性参数——如启动力与滑动力(BLGF)及注射时间——则高度依赖于药物制剂的物理特性。尽管如此,供应商仍可依据药企合作伙伴提供的制剂数据,对这些参数进行前瞻性的模拟评估。
此类预先评估使供应商能够在针对特定药物的测试启动之前,识别潜在风险、优化组件的匹配度并确保符合相关标准(图2)。通过运用平台性能数据,供应商可为药械组合产品推荐最合适的材料和组件。这些早期共享的数据不仅有助于简化开发流程,还能降低制药公司在选择初级容器时的风险,减少了代价高昂的设计迭代,并加快了产品上市时间。
非药物相关型与药物依赖型注射器的系统特性
自动注射器中的预灌封注射器(PFS)具备若干非药物相关(Liquid-Agnostic)的基础特性,这些特性必须经过测试和验证。此类特性包括:尺寸配合度、针头护帽移除力、激活力(选择合适的弹簧)以及穿刺力(取决于针头外径和规格)。相比之下,药物依赖型自动注射器(已集成预灌封注射器)系统特性则更为复杂,例如:剂量准确性、实际给药量、平均滑动力以及注射时间。针头内径、药液粘度、药液密度、温度以及针头伸出长度等因素,均会显著影响系统的功能性。
Gerresheimer、SHL Medical 和 Aptar Pharma 在一项联合研究中,对平均滑动力和注射时间这两项药物依赖型的性能特征进行了测试。与图 3 所示的拔出力(PoF)测试一样,本次测试使用了一支 2.25 mL 的 Gx® Elite 注射器,配备 27G 薄壁针头(内径 0.28 mm)。注射器内灌装了粘度为 15 cP 的甘油溶液,采用 Aptar Pharma 的 PremiumCoat® 活塞进行加塞,并组装到 SHL Medical 的 Molly® 自动注射器中。测试结果显示,在 0.5 mm/s 的速度下,平均滑动力为 3.66 N;而在 5 mm/s 的较高注射速度下,平均滑动力为 33.01 N。在该系统配置下,测得的注射时间为 9.41 秒,这是自动注射器应用中常用的目标值(见图 4)。

结论
SHL Medical、Aptar Pharma 和格雷斯海姆共同印证了制药公司与组件供应商之间的协作,对于成功开发基于自动注射器的药械组合产品起着至关重要的作用。早期获取的与药物相关的信息越多,推荐适配的自动注射器系统就越容易。从注射器针筒、弹性体组件到自动注射器本身,每一个部件都必须经过精密设计并实现无缝集成,以满足当今组合型药物输送系统严苛的性能与法规要求。
供应商与制药合作伙伴之间的紧密合作,不仅能够及早识别与药物无关的性能因素,还能支持全面的风险评估,并提供对强大平台数据的访问权限。这不仅有助于降低组件(如活塞、针头护帽及初级容器)选型的风险,还能加快开发进程,减少在后期进行昂贵设计变更的需求。
通过运用各自领域的专业知识,供应商能够推荐针对制药需求量身定制的优化材料与配置。制药公司则能从数据驱动的决策中获益,并更高效地推进开发与监管过程中的各个关键节点。最终,所形成的组合产品不仅安全有效,而且兼具以患者为中心的设计理念和商业可行性。
综上所述,药械、组件供应商及制药企业各方利益相关者之间的无缝协作,为创新、效率与长期成功奠定了坚实基础,从而打造出真正发挥协同增效(1+1>2)价值的解决方案。












